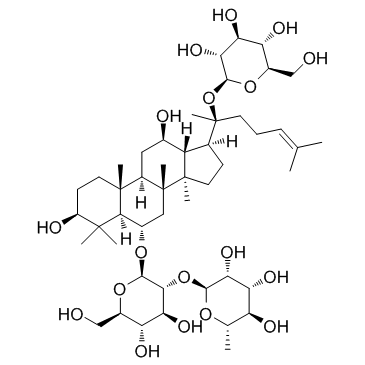
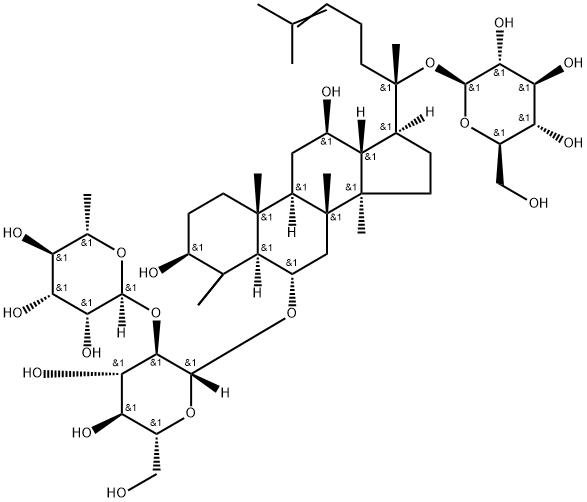
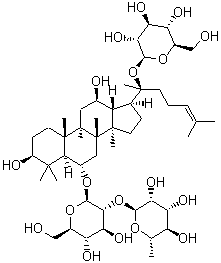
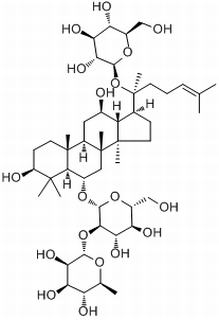
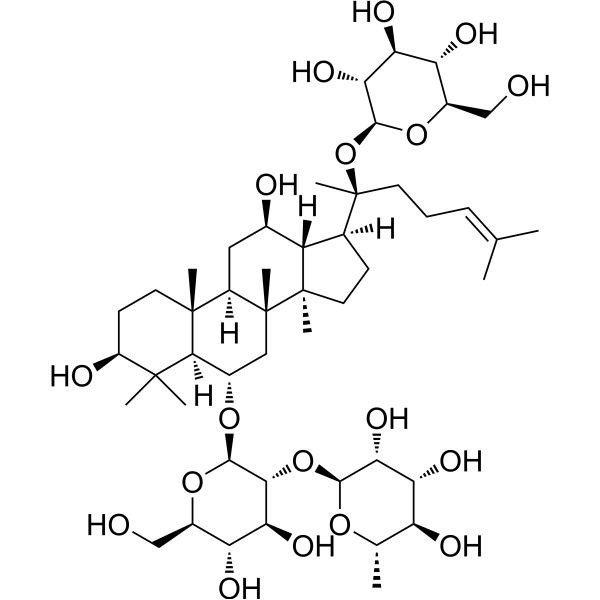
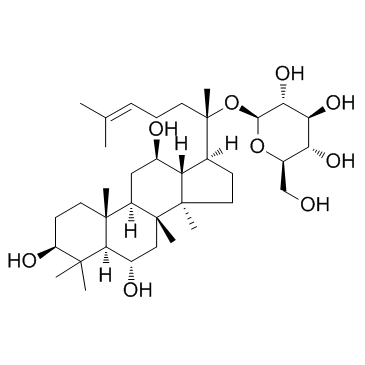
人参皂苷Re,Ginsenoside Re,分析标准品,HPLC≥99%
产品编号:Bellancom-YE13063| CAS NO:52286-59-6| MDL NO:MFCD00133369| 分子式:C48H82O18| 分子量:947.15
Ginsenoside Re 是一种 Panax notoginseng 提取物。 Ginsenoside Re 可降低 β-淀粉样蛋白 (Aβ)。Ginsenoside Re 还通过抑制 JNK 和 NF-κB 发挥抗炎作用。
本网站销售的所有产品仅用于工业应用或者科学研究等非医疗目的,不可用于人类或动物的临床诊断或者治疗,非药用,非食用,
| 英文名称 | Ginsenoside Re | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CAS编号 | 52286-59-6 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品描述 | Ginsenoside Re 是一种 Panax notoginseng 提取物。 Ginsenoside Re 可降低 β-淀粉样蛋白 (Aβ)。Ginsenoside Re 还通过抑制 JNK 和 NF-κB 发挥抗炎作用。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品熔点 | 202 °C(dec.) | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品沸点 | 1011.8±65.0 °C at 760 mmHg | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品密度 | 1.4±0.1 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品闪点 | 565.7±34.3 °C | |||||||||||||||||||||||||||||||||||||||||||||||
| 精确质量 | 946.550110 | |||||||||||||||||||||||||||||||||||||||||||||||
| PSA | 298.14000 | |||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 4.75 | |||||||||||||||||||||||||||||||||||||||||||||||
| 外观性状 | 白色晶体 | |||||||||||||||||||||||||||||||||||||||||||||||
| 蒸气压 | 0.0±0.6 mmHg at 25°C | |||||||||||||||||||||||||||||||||||||||||||||||
| 折射率 | 1.611 | |||||||||||||||||||||||||||||||||||||||||||||||
| 溶解性 | 可溶于水、热甲醇、乙醇等溶剂,不溶于石油醚。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 溶解性数据 | In Vitro:
DMSO : ≥ 50 mg/mL (52.79 mM) * "≥" means soluble, but saturation unknown. 配制储备液
*
请根据产品在不同溶剂中的溶解度选择合适的溶剂配制储备液;一旦配成溶液,请分装保存,避免反复冻融造成的产品失效。 In Vivo:
请根据您的实验动物和给药方式选择适当的溶解方案。以下溶解方案都请先按照 In Vitro 方式配制澄清的储备液,再依次添加助溶剂:
——为保证实验结果的可靠性,澄清的储备液可以根据储存条件,适当保存;体内实验的工作液,建议您现用现配,当天使用;
以下溶剂前显示的百
| |||||||||||||||||||||||||||||||||||||||||||||||
| 靶点 |
Aβ1-40 Aβ1-42 NF-κB JNK | |||||||||||||||||||||||||||||||||||||||||||||||
| 体外研究 | 人参皂苷Re是一种着名的中药,它可以降低β位点淀粉样蛋白前体蛋白裂解酶1(BACE1)的mRNA和蛋白水平,并抑制N2a / APP695细胞中的BACE1活性。人参皂苷Re还显着增加PPARγ蛋白和mRNA水平。为了防止人参皂苷Re对N2a / APP695细胞具有细胞毒性作用,首先通过MTT测定确定细胞活力。用递增浓度的人参皂苷Re(0-200μM)处理N2a / WT和N2a / APP695细胞24小时。低于100μM的人参皂苷Re浓度不影响N2a / WT和N2a / APP695细胞的活力,而150μM人参皂苷Re浓度显着降低N2a / WT和N2a / APP695细胞的存活率。与人参皂苷Re在200μM浓度下孵育24小时分别使N2a / WT和N2a / APP695细胞的存活率降低15.58%和26.82%。这些数据表明,人参皂甙Re处理在0-100μM范围内24小时对N2a / WT和N2a / APP695细胞是安全的(P> 0.05)。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 体内研究 | 人参皂甙Re通过抑制JNK和NF-κB活化来降低3T3-L1脂肪细胞和高脂饮食(HFD)大鼠的胰岛素抵抗。以20mg / kg的剂量腹膜内注射脂多糖(LPS)对小鼠是致命的,并且70%至80%的小鼠在60小时内死亡。然而,用Rg1或人参皂苷Re预处理小鼠以剂量依赖性方式增加其存活率。随着Rg1或人参皂苷Re的剂量从2.5mg / kg增加至5mg / kg,存活率从60%升高至90%(Rg1)或从30%升高至40%(人参皂苷Re)。与用等剂量的人参皂苷Re处理的小鼠的80%存活率相比,以10mg / kg的最小剂量施用Rg1的所有小鼠都免于死亡。为了保护所有小鼠,需要20mg / kg人参皂苷Re。为了研究Rg1和人参皂苷Re的抗炎潜力,将1mg / kg Rg1或人参皂苷Re注射到大鼠中,然后用LPS攻击动物。注射过程本身导致每组中瞬时应力引起的体温升高~1.2℃。此后,未经预处理的LPS攻击的大鼠发展出强烈的双相发热,第一峰在2小时达到~1.5℃,第二峰在4小时达到1.8℃。相反,Rg1-,人参皂苷Re-和TAK-242-处理组的温度变化在2小时仅为0.9,1.2和0.8℃,在4小时时分别为1.3,1.4和1.0℃。用Rg1,人参皂苷Re或TAK-242预处理可显着减弱LPS诱导的体温变化。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 细胞实验 | 为了探索人参皂苷Re对N2a / APP695细胞的细胞毒性作用,使用MTT测定评估细胞增殖。用增加剂量的人参皂苷Re(0,25,50,100,150和200μM)处理细胞24小时。在处理后进行MTT测定。将细胞在37℃下与溶解在新鲜完全培养基中的0.5mg / mL MTT一起温育4小时。将深蓝色甲crystals晶体溶解在DMSO中,并使用630nm的参考波长和490nm的测试波长在酶标仪上测量吸光度。数据表示为活细胞与对照的平均百分比。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 动物实验 |
*下述溶液配置方法仅为基于分子量计算出的理论值。不同产品在配置溶液前,需考虑其在不同溶剂中的溶解度限制。
不同实验动物依据体表面积的等效剂量转换表(参考来源于公开文献)
例如,依据体表面积折算法,将化合物用于小鼠的剂量20 mg/kg 换算成大鼠的剂量,需要将20 mg/kg 乘以小鼠的Km系数(3),再除以大鼠的Km系数(6),得到化合物用于大鼠的等效剂量为10 mg/kg。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 稳定性 | 如果遵照规格使用和储存则不会分解,未有已知危险反应 | |||||||||||||||||||||||||||||||||||||||||||||||
| 储存条件 | 保持贮藏器密封、储存在阴凉、干燥的地方,确保工作间有良好的通风或排气装置 |
相关文档
化学品安全说明书(MSDS)
下载MSDS质检证书(COA)
相关产品
| 危害码 (欧洲) | Xn: Harmful; |
|---|---|
| 风险声明 (欧洲) | R20/21/22 |
| 安全声明 (欧洲) | 26-36 |
| 危险品运输编码 | NONH for all modes of transport |
| WGK德国 | 3 |
| RTECS号 | LY9536700 |
| 产品名: | Ginsenoside-Re |
| CAS号: | 52286-59-6 |
| 制造商/供应商: | 西域试剂 网站:www.hzbp.cn 邮件:13911702513@139.com |
2. 合成/成分数据
| 产品名: | Ginsenoside-Re |
| 别名: | Ginsenoside B2; Panaxoside Re; Chikusetsusaponin IVc; Sanchinoside Re |
| 分子式: | C48H82O18 |
| 分子量: | 947.14 |
3. 急救措施
| 吸入后: | 如果吸入,移至空气新鲜处,如果呼吸困难,给输氧,如呼吸停止,给予人工呼吸。 |
| 皮肤接触后: | 用大量的水冲洗,移除污染的衣服和鞋子。 |
| 眼睛接触后: | 检查并取下隐形眼镜,并用大量的水冲洗;呼叫医生。 |
| 吞食后: | 如果吞食,用大量纯净水漱口;呼叫医生。 |
4. 消防措施
| 适当的灭火剂: | 雾状水,二氧化碳,干粉或泡沫。 |
| 防护设备: | 穿戴自给式呼吸器和防护服,以防止与皮肤和眼睛接触。 |
5. 泄漏应急处理
| 安全防范措施: | 封锁泄漏区域;穿戴自给式呼吸器,防护服和厚橡胶手套。 |
| 清洁/收集措施: | 使用液体粘合原料(硅藻土,通用粘合剂)吸取精细粉末; 使用酒精擦洗表面和设备除去污渍; 根据第11条处理被污染的材料。 |
6. 处理和储存
| 安全处理说明: | 避免吸入和接触皮肤,眼睛及衣物;材料可能略微具有刺激性。 |
| 储存: |
粉末型式 -20°C 3年;4°C 2年 溶于溶剂 -80°C 6个月;-20°C 1个月 |
7. 接触控制和个人防护
| 呼吸设备: | NIOSH / MSHA认可的呼吸器。 |
| 双手保护: | 耐化学腐蚀的橡胶手套。 |
| 眼睛防护: | 化学安全护目镜。 |
8. 稳定性和反应活性
| 稳定性: | 按照说明存储是稳定的;避免强氧化剂。 |
| 热分解/其他要避免的情况: | 避免光和热。 |
9. 毒性资料
| 急性毒性: | 无可用资料。 |
| 主要刺激性影响: | 无可用资料。 |
| 在皮肤上: | 无可用资料。 |
| 对眼睛: | 无可用资料;可能具有刺激性。 |
10. 生态资料
| 一般注意事项: | 无可用资料。 |
11. 废弃处置
| 按照所在国家,省份,县市和地方的法规处置。 |
12. 运输信息
| 正确的运输名称: | 无 |
| 非危险品运输: | 这种物质被视为非危险品运输。 |
13. 法规信息
| 尚未有针对此产品作出的化学安全性评估。 |
14. 其他信息
| 这种化学品仅供受过训练的,有经验的研究人员在穿戴适当装备和授权允许的情况下进行操作处理。以上信息基于我们目前的知识被认为是正确的,但只适用于作为有经验人员的指导。请咨询您自己的安全顾问,并遵守当地和国家的安全法规。在任何其他没有被警告的情况下,并不意味着绝对没有危险存在。西域生物技术不承担任何使用这种化学品所造成的损害和责任。2023 西域生物技术版权所有。 |
|
~% 
52286-59-6 |
| 文献:Morita; Kong; But; et al. Chemical and Pharmaceutical Bulletin, 1986 , vol. 34, # 10 p. 4368 - 4372 |
| 上游产品 0 | |
|---|---|
| 下游产品 5 | |
- 49. Yongshen Ren, Jiao Ai, Xinqiao Liu, Shuai Liang, Yao Zheng, Xin Deng, Yan Li, Jing Wang, Xukun Deng, Lin-Lin Chen, Anticoagulant active ingredients identification of total saponin extraction of different Panax medicinal plants based on grey relational anal
- 48. Chen, Jiali, et al. "Ginsenosides and amino acids in flavored ginseng chips as affected by food formulation and processing technology." LWT-Food Science and Technology 62.1 (2015): 517-524.https://doi.org/10.1016/j.lwt.2014.10.047
- 47. Manying Wang, Jixiang Ren, Xuenan Chen, Jianzeng Liu, Xiaohao Xu, Xiangyan Li, Daqing Zhao, Liwei Sun, 20(S)-ginsenoside Rg3 promotes myoblast differentiation and protects against myotube atrophy via regulation of the Akt/mTOR/FoxO3 pathway, Biochemical Ph
- 46. Yu, Jingping, et al. "Comprehensive Quality Evaluation of American Ginseng for Different Parts and Abnormal Trait Based on the Major Ginsenoside Contents and Morphological Characteristics." BioMed research international 2021 (2021).https://doi.org/10.1155/
- 45. Joo, Kyung-Mi, et al. "Pharmacokinetic study of ginsenoside Re with pure ginsenoside Re and ginseng berry extracts in mouse using ultra performance liquid chromatography/mass spectrometric method." Journal of pharmaceutical and biomedical analysis 51.1 (20
- 44. Jin, Wenqi, et al. "Ginsenoside Rd attenuates ACTH-induced corticosterone secretion by blocking the MC2R-cAMP/PKA/CREB pathway in Y1 mouse adrenocortical cells." Life sciences 245 (2020): 117337.https://doi.org/10.1016/j.lfs.2020.117337
- 43. 邵紫君,李志满,于鹏程,陈建波,李珊珊,孙印石.氨基酸转化三七花中稀有人参皂苷及提取液对脂多糖诱导的RAW264.7细胞活性的影响[J].中草药,2021,52(03):702-710.
- 42. 张娜,黄鑫,郭云龙,越皓,刘淑莹.基于UPLC-QQQ-MS多指标统计分析研究不同生境人参中皂苷分布[J].特产研究,2020,42(06):48-54.
- 41. 温宝庆,李文庆,周妙霞,林坤霞,汪小东,钱正明.茯神饮中化学成分的核壳色谱-四级杆飞行时间质谱联用鉴定和分析[J].时珍国医国药,2020,31(06):1334-1338.
- 40. 胡小松. 五灵脂中菌群种类及其生物转化作用初步研究[D].北京中医药大学,2020.
- 39. 屈青松,林峰,赵崇妍,马涛,宋帅,史新元.发酵乳杆菌发酵人参工艺优化及人参皂苷抗氧化活性测定[J].中成药,2020,42(10):2738-2743.
- 38. 范琳,王苗,马馨桐,沈颖昕,韩荣欣,张红印,严铭铭,邵帅.葛根抗氧化活性有效部位的筛选研究[J].食品研究与开发,2021,42(06):119-123.
- 37. 张涛,王冠,张维维,陈湘,张庆贺,刘芳馨,李卓然,齐伟辰.温度调控对人参皂苷积累及其关键酶基因表达的影响[J].中草药,2020,51(19):5035-5040.
- 36. 屈文佳,贾天颖,王海丽,辛洁萍,王敏,白玉莹,徐文娟,李向日.不同蒸制时间下红参颜色及3种常见人参皂苷的转化规律研究[J].北京中医药大学学报,2020,43(09):769-775.
- 35. 谢果珍,唐圆,姜珊,罗帅,谭周进.七味白术散总苷的提取工艺优化及体外抑菌活性初探[J].时珍国医国药,2020,31(06):1351-1354.
- 34. 吴冬雪,王秋颖,王淑敏,陈思键,刘淑莹,赵幻希,修洋.人参皂苷的仿生提取研究[J].分析试验室,2021,40(02):145-149.
- 33. 王艳,尉忠贤,李晶.HPLC法测定不同厂家振源片中人参皂苷的含量[J].西北药学杂志,2020,35(05):669-673.
- 32. 杜静. 冠突散囊菌对中药材三七成分的转化及机理研究[D].贵州师范大学,2020.
- 31. 越皓,周东月,张美玉,张琰,戴雨霖,郑飞,朱英豪.红参中原人参三醇型皂苷组在肠道菌群中体外转化及对肠道菌群的作用[J].应用化学,2021,38(03):323-330.
- 30. 李雪晴, 李丽, 刘秀峰,等. 三七皂苷的人肠道菌群体外代谢研究[J]. 药物生物技术, 2017(03):34-39.
- 29. 夏晚霞, 张尚微, 葛亚中,等. 乳酸菌发酵转化人参皂苷[J]. 现代食品科技, 2018, 34(09):136-142.
- 28. 李灿, 唐利军, 茹琴,等. 戒毒一号的高效液相色谱指纹图谱研究[J]. 江汉大学学报(自然科学版), 2018, 46(05):471-476.
- 27. 杨林, 徐晓珍, 陈劲柏,等. UHPLC法同时测定参麦注射液中8种人参皂苷[J]. 中成药, 2019.
- 26. 赵昶灵, 杨生超, 陈中坚,等. 紫,绿三七的总花色苷和总皂苷含量及皂苷单体组成[J]. 中药材, 2014, 37(10):1749-1753.
- 25. 苗瑞, 吴冬雪, 王秋颖,等. 基于多壁碳纳米管的人参皂苷快速分离[J]. 高等学校化学学报, 2018.
- 24. 张艳欣, 朱国琴, 王丹丹. 均匀设计法优化林下山参中人参皂苷提取工艺的研究[J]. 上海医药, 2019, 040(015):89-92.
- 23. 吴冬雪,刘淑莹,陈思键,赵幻希,修洋,王淑敏.固相萃取结合高效液相色谱-三重四极杆质谱快速分离检测益气养血口服液中人参皂苷的新方法[J].分析测试学报,2020,39(07):867-873.
- 22. 吴雨佳, 王令充, 张雯,等. 生物黏附性三七总皂苷-白及多糖-海藻酸钠复合微球的制备及表征[J]. 中草药, 2019, v.50;No.655(20):49-56.
- 21. 郑尧. 人参鲜药干制/复水过程水分状态与化学成分变化规律研究[J]. 中草药 2019(14):3302-3312.
- 20. 王灿灿 戴黎蓉 赵旻 等. UPLC法同时测定四君子汤中7种化学成分的含量[J]. 沈阳药科大学学报 2018 v.35;No.271(08):639-645.
- 19. 张永 陈旭 丁越 等. HPLC法结合统计学方法研究复方丹参片中皂苷类成分[J]. 辽宁中医杂志 2019 46(01):126-129.
- 18. 赵立春 刘继永. Box-Behnken法优化人参皂苷Rg1 Re Rb1提取工艺[J]. 食品工业 2020(1).
- 17. 张琰, 李方彤, 韩铭鑫,等. 通过RRLC-Q-TOF MS和UPLC-QQQ MS分析原人参三醇型皂苷在人肠道菌群中的代谢产物[J]. 质谱学报, 2020(1):66-75.
- 16. 陶雪慧 王安琪 王康宇 等. 五味子胶囊提取工艺研究[J]. 长春中医药大学学报 2018(4):659-662.
- 15. 余健, 徐晓珍, 顾利强,等. 高效液相色谱-串联质谱法同时测定参麦注射液中9种皂苷[J]. 中华中医药学刊, 2014.
- 14. 李晶, 朱娜, 郑飞,等. 红参红景天混合物提取工艺及其抗疲劳作用[J]. 食品工业科技, 2019, 040(016):181-185,191.
- 13. 杨丽颖 郭伟英. HPLC-ELSD法同时测定益心宁神片中5种成分的含量[J]. 中药材 2015 38(012):2619-2622.
- 12. 宁张弛 刘振丽 宋志前 等. HPLC-QqQ-MS测定珠子参中5种皂苷类成分的含量[J]. 中国中药杂志 2016 v.41(05):874-878.
- 11. 李雯, 韩惠敏, 赵天煜,等. 黑米花青苷复方软胶囊生产工艺研究[J]. 粮食流通技术, 2018, 000(007):149-152.
- 10. 李雯, 李新生, 赵冠杰,等. 黑米花青苷复方软胶囊有效成分抗氧化活性研究[J]. 食品科技, 2018, 43(10):114-120.
- 9. 戴浩, 张晓伟, 李风涛,等. 酶解组合高速匀浆法提取人参总皂苷和多糖[J]. 保鲜与加工, 2020, v.20;No.118(03):145-153.
- 8. 程璐, 谢翔, 刘中原,等. 海参水煮液皂苷的美白抗衰老功效[J]. 精细化工, 2018, 35(002):267-271,290.
- 7. 付佳 苑广信 安丽萍 等. 双参颗粒剂的制备[J]. 时珍国医国药 2018 29(3):598-600.
- 6. 乐 王维肖 杨贺旻 等. 人参皂苷Re对吗啡依赖戒断后小鼠抑郁样行为的影响[J]. 延边大学医学学报 2019(2).
- 5. 田静 任雨贺 刘淑莹 等. 人参皂苷Rc Rd Re对神经胶质瘤细胞增殖作用的影响[J]. 中成药 2020 042(003):751-754.
- 4. 杜琳 刘知源 赵凌志. 人参果皂苷前体阳离子脂质体的制备及体外释放研究[J]. 吉林中医药 2017(10).
- 3. 黄晓兵 李积华 彭芍丹 et al. 五个产地荔枝核中药饮片抗氧化活性研究[J]. 食品工业科技 2014 35(022):91-94.
- 2. 孙雨薇 王珊珊 徐浩 等. 不同方法对人参皂苷Re提取效果的影响[J]. 食品工业科技 2014 35(014):301-304.
- 1. 王震 马伟 李洪源 等. 三个不同产地人参中皂苷含量的差异性研究[J]. 中医药信息 2019 036(003):83-86.







 浙公网安备 33010802013016号
浙公网安备 33010802013016号