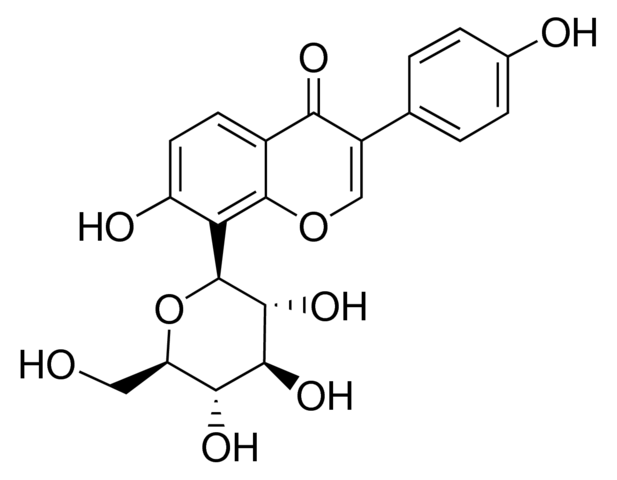
葛根素,Puerarin,分析标准品,HPLC≥99%
产品编号:Bellancom-YE12506| CAS NO:3681-99-0| MDL NO:MFCD00076007| 分子式:C21H20O9| 分子量:416.38
葛根素是一种黄酮类化合物,从传统的东方药物葛根。Purarin具有潜在的抗氧化活性,可破坏CYP催化的药物代谢。一种代谢物,毛蕊异黄酮,具有细胞毒活性。葛根素预防慢性酒精中毒对空间学习记忆能力的影响主要是由于其抗炎活性和对谷氨酸和氨基丁酸平衡的调节。葛根素可能通过促进骨形成和NO/cGMP通路来预防骨质疏松,这在葛根素诱导的hBMSC增殖和成骨细胞分化中起重要作用。
本网站销售的所有产品仅用于工业应用或者科学研究等非医疗目的,不可用于人类或动物的临床诊断或者治疗,非药用,非食用,
| 产品名称 | 葛根素 | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 英文名称 | Puerarin | |||||||||||||||||||||||||||||||||||||||||||||||
| CAS编号 | 3681-99-0 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品描述 | 葛根素是一种黄酮类化合物,从传统的东方药物葛根。Purarin具有潜在的抗氧化活性,可破坏CYP催化的药物代谢。一种代谢物,毛蕊异黄酮,具有细胞毒活性。葛根素预防慢性酒精中毒对空间学习记忆能力的影响主要是由于其抗炎活性和对谷氨酸和氨基丁酸平衡的调节。葛根素可能通过促进骨形成和NO/cGMP通路来预防骨质疏松,这在葛根素诱导的hBMSC增殖和成骨细胞分化中起重要作用。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品熔点 | 187-189°C | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品沸点 | 791.2±60.0 °C at 760 mmHg | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品密度 | 1.6±0.1 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||
| 产品闪点 | 281.5±26.4 °C | |||||||||||||||||||||||||||||||||||||||||||||||
| 精确质量 | 432.105652 | |||||||||||||||||||||||||||||||||||||||||||||||
| PSA | 160.82000 | |||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0.67 | |||||||||||||||||||||||||||||||||||||||||||||||
| 外观性状 | 白色针状结晶 | |||||||||||||||||||||||||||||||||||||||||||||||
| 蒸气压 | 0.0±2.9 mmHg at 25°C | |||||||||||||||||||||||||||||||||||||||||||||||
| 折射率 | 1.717 | |||||||||||||||||||||||||||||||||||||||||||||||
| 溶解性 | DMSO : 50 mg/mL (120.08 mM; Need ultrasonic) | |||||||||||||||||||||||||||||||||||||||||||||||
| 溶解性数据 | In Vitro:
DMSO : 50 mg/mL (120.08 mM; Need ultrasonic) 配制储备液
*
请根据产品在不同溶剂中的溶解度选择合适的溶剂配制储备液;一旦配成溶液,请分装保存,避免反复冻融造成的产品失效。 In Vivo:
请根据您的实验动物和给药方式选择适当的溶解方案。以下溶解方案都请先按照 In Vitro 方式配制澄清的储备液,再依次添加助溶剂:
——为保证实验结果的可靠性,澄清的储备液可以根据储存条件,适当保存;体内实验的工作液,建议您现用现配,当天使用;
以下溶剂前显示的百
| |||||||||||||||||||||||||||||||||||||||||||||||
| 体外研究 | 葛根素抑制LPS诱导的iNOS,COX-2和CRP蛋白的表达,并且还抑制其在RAW264.7细胞中的RT-PCR实验中的mRNA。 iNOS,COX-2和CRP表达的抑制是由于磷酸化和I-κB降解的剂量依赖性抑制,导致p65NF-κB核转位的减少。葛根素介导的抑制LPS诱导的iNOS,COX-2和CRP表达的作用归因于在转录水平上抑制NF-κB活化。葛根素是一种新型的IK1开放通道阻滞剂,可能是葛根素抗心律失常作用的基础。葛根素与IK1的开放通道阻滞剂钡竞争抑制IK1电流。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 体内研究 | 金雀异黄素和葛根素均可通过潜在的抗氧化,抗炎或抗凋亡机制有效缓解慢性酒精引起的肝损伤。然而,金雀异黄素在降低丙二醛水平方面比葛根素更有效(1.05±0.0947对比1.28±0.213 nmol / mg pro,p <0.05),肿瘤坏死因子α(3.12±0.498对3.82±0.277 pg / mg pro, p <0.05),白细胞介素-6(1.46±0.223对1.88±0.309 pg / mg pro,p <0.05),而葛根素在改善血清活性或丙氨酸转氨酶水平方面比金雀异黄素更有效(35.8±3.95 vs. 42.6) ±6.56 U / L,p <0.05)和低密度脂蛋白胆固醇(1.12±0.160对1.55±0.150 mmol / L,p <0.05)。葛根素可显着改善早期肾损害,可能通过抑制糖尿病大鼠肾脏中ICAM-1和TNF-α的表达。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 细胞实验 | RAW264.7细胞在95%空气和5%CO 2湿润气氛中维持在37℃的亚汇合状态。用于常规传代培养的培养基是Dulbecco's Modified Eagle's培养基,其补充有10%胎牛血清,青霉素(100单位/ mL)和链霉素(100μg/ mL)。 MTT测定用于测量用葛根素处理后细胞的活力。除去上清液用于亚硝酸盐测定后,将细胞在37℃下与MTT(0.05mg / mL)一起温育4小时,并在540nm处测量光密度。葛根素的浓度分别为10,20,40和100μM。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 动物实验 |
*下述溶液配置方法仅为基于分子量计算出的理论值。不同产品在配置溶液前,需考虑其在不同溶剂中的溶解度限制。
不同实验动物依据体表面积的等效剂量转换表(参考来源于公开文献)
例如,依据体表面积折算法,将化合物用于小鼠的剂量20 mg/kg 换算成大鼠的剂量,需要将20 mg/kg 乘以小鼠的Km系数(3),再除以大鼠的Km系数(6),得到化合物用于大鼠的等效剂量为10 mg/kg。 | |||||||||||||||||||||||||||||||||||||||||||||||
| 稳定性 | 常温常压下稳定,白色针状结晶 | |||||||||||||||||||||||||||||||||||||||||||||||
| 储存条件 | 储存条件 2-8°C, dry, sealed 运输方式 冰袋运输,根据产品的不同,可能会有相应调整。 |
相关文档
化学品安全说明书(MSDS)
下载MSDS质检证书(COA)
相关产品
| 个人防护装备 | Eyeshields;Gloves;type N95 (US);type P1 (EN143) respirator filter |
|---|---|
| 危害码 (欧洲) | F,C |
| 风险声明 (欧洲) | R11 |
| 安全声明 (欧洲) | 22-24/25-45-36/37/39-26-16 |
| 危险品运输编码 | NONH for all modes of transport |
| WGK德国 | 3 |
| RTECS号 | UO5216000 |
| 海关编码 | 2932999099 |
| 产品名: | Puerarin |
| CAS号: | 3681-99-0 |
| 制造商/供应商: | 西域试剂 网站:www.hzbp.cn 邮件:13911702513@139.com |
2. 合成/成分数据
| 产品名: | Puerarin |
| 分子式: | C21H20O9 |
| 分子量: | 416.38 |
3. 急救措施
| 吸入后: | 如果吸入,移至空气新鲜处,如果呼吸困难,给输氧,如呼吸停止,给予人工呼吸。 |
| 皮肤接触后: | 用大量的水冲洗,移除污染的衣服和鞋子。 |
| 眼睛接触后: | 检查并取下隐形眼镜,并用大量的水冲洗;呼叫医生。 |
| 吞食后: | 如果吞食,用大量纯净水漱口;呼叫医生。 |
4. 消防措施
| 适当的灭火剂: | 雾状水,二氧化碳,干粉或泡沫。 |
| 防护设备: | 穿戴自给式呼吸器和防护服,以防止与皮肤和眼睛接触。 |
5. 泄漏应急处理
| 安全防范措施: | 封锁泄漏区域;穿戴自给式呼吸器,防护服和厚橡胶手套。 |
| 清洁/收集措施: | 使用液体粘合原料(硅藻土,通用粘合剂)吸取精细粉末; 使用酒精擦洗表面和设备除去污渍; 根据第11条处理被污染的材料。 |
6. 处理和储存
| 安全处理说明: | 避免吸入和接触皮肤,眼睛及衣物;材料可能略微具有刺激性。 |
| 储存: |
粉末型式 -20°C 3年;4°C 2年 溶于溶剂 -80°C 6个月;-20°C 1个月 |
7. 接触控制和个人防护
| 呼吸设备: | NIOSH / MSHA认可的呼吸器。 |
| 双手保护: | 耐化学腐蚀的橡胶手套。 |
| 眼睛防护: | 化学安全护目镜。 |
8. 稳定性和反应活性
| 稳定性: | 按照说明存储是稳定的;避免强氧化剂。 |
| 热分解/其他要避免的情况: | 避免光和热。 |
9. 毒性资料
| 急性毒性: | 无可用资料。 |
| 主要刺激性影响: | 无可用资料。 |
| 在皮肤上: | 无可用资料。 |
| 对眼睛: | 无可用资料;可能具有刺激性。 |
10. 生态资料
| 一般注意事项: | 无可用资料。 |
11. 废弃处置
| 按照所在国家,省份,县市和地方的法规处置。 |
12. 运输信息
| 正确的运输名称: | 无 |
| 非危险品运输: | 这种物质被视为非危险品运输。 |
13. 法规信息
| 尚未有针对此产品作出的化学安全性评估。 |
14. 其他信息
| 这种化学品仅供受过训练的,有经验的研究人员在穿戴适当装备和授权允许的情况下进行操作处理。以上信息基于我们目前的知识被认为是正确的,但只适用于作为有经验人员的指导。请咨询您自己的安全顾问,并遵守当地和国家的安全法规。在任何其他没有被警告的情况下,并不意味着绝对没有危险存在。西域生物技术不承担任何使用这种化学品所造成的损害和责任。2023 西域生物技术版权所有。 |
|
~71% 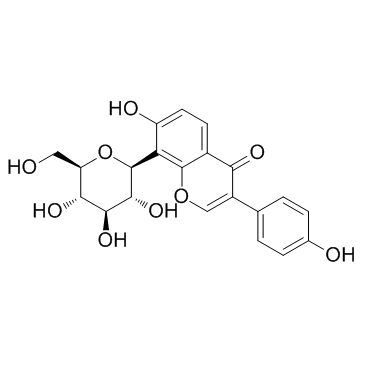
3681-99-0 |
| 文献:Kato, Eisuke; Kawabata, Jun Bioorganic and Medicinal Chemistry Letters, 2010 , vol. 20, # 15 p. 4333 - 4336 |
|
~76% 
3681-99-0 |
| 文献:Lee; Ji; Zhang Journal of Labelled Compounds and Radiopharmaceuticals, 2007 , vol. 50, # 8 p. 702 - 705 |
|
~% 
3681-99-0 |
| 文献:Lee, David Y. W.; Zhang, Wu-Yan; Karnati, Vishnu Vardhan R. Tetrahedron Letters, 2003 , vol. 44, # 36 p. 6857 - 6859 |
|
~% 
3681-99-0 |
| 文献:Park; Hakamatsuka; Noguchi; Sankawa; Ebizuka Chemical and Pharmaceutical Bulletin, 1992 , vol. 40, # 7 p. 1978 - 1980 |
- 72. [IF=2.826] Kai Sheng et al."Simple voltammetric sensor detection for puerarin."Int J Environ An Ch. 2021;101(12):1635-1648
- 55. [IF=3.361] Hongguang Zhang et al."Extraction of isoflavones from Puerariae lobata using subcritical water."Rsc Adv. 2018 Jun;8(40):22652-22658
- 52. [IF=5.396] Song Liu et al."The in silico and in vivo evaluation of puerarin against Alzheimer's disease."Food Funct. 2019 Feb;10(2):799-813
- 49. Yu, Yunru, et al. "Identification of anti-inflammatory compounds from Zhongjing formulae by knowledge mining and high-content screening in a zebrafish model of inflammatory bowel diseases." Chinese medicine 16.1 (2021): 1-14.
- 48. Zhang, Jifen, et al. "Development of an oral compound pickering emulsion composed of nanocrystals of poorly soluble ingredient and volatile oils from traditional chinese medicine." Pharmaceutics 10.4 (2018): 170.https://doi.org/10.3390/pharmaceutics1004017
- 47. Huang, W, Wen, Z, Wang, M, Xu, B, Zhou, B, Li, X. Anticomplement and antitussive activities of major compound extracted from Chimonanthus nitens Oliv. leaf. Biomedical Chromatography. 2020; 34:e4736. https://doi.org/10.1002/bmc.4736
- 46. Li, Na, et al. "Comparative Tissue Distribution of 6 Major Polyphenolic Compounds in Normal and Myocardial Ischemia Model Rats After Oral Administration of the Polygonum orientale L. Extract." Natural Product Communications 15.6 (2020): 1934578X20929447.ht
- 45. Renshu, Huang, et al. "Extraction technology of isoflavone from Dabie Mountain's Pueraria lobata and determination of its reducing power." Pakistan journal of pharmaceutical sciences 27 (2014).
- 44. Shasha Jing, Huijun Zheng, Li Zhao, Lingbo Qu, Lanlan Yu, A novel electrochemical sensor based on WO3 nanorods-decorated poly(sodium 4-styrenesulfonate) functionalized graphene nanocomposite modified electrode for detecting of puerarin, Talanta, Volume 174
- 43. 李承浩,王萌,任晓亮.磺化杯6芳烃对4类中药单体成分增溶作用及其机制研究[J].中国现代中药,2020,22(12):2032-2038.
- 42. 鞠娜,张文风,翁丽丽.正交实验法优选玉液汤提取工艺[J].特产研究,2021,43(01):7-11.
- 41. 陈函,廉婷,杜远东,陈程,马宝.鼻用葛根素脂质体温敏凝胶剂的制备与质量评价[J].化工科技,2020,28(05):41-46.
- 40. 刘春花,王明金,杨淑婷,黎娜,陆苑,潘洁,李勇军,王永林,孙佳.基于外翻肠囊模型研究荭草提取物在正常和心肌缺血模型大鼠中的肠吸收特征[J].中国中药杂志,2021,46(01):196-205.
- 39. 王晶,赵重博,唐家琪,卜雕雕,邹俊波,张小飞,程江雪,王昌利.高效液相色谱法同时测定复方龙脉宁中7种成分的含量[J].中南药学,2020,18(11):1903-1905.
- 38. 范琳,王苗,马馨桐,沈颖昕,韩荣欣,张红印,严铭铭,邵帅.葛根抗氧化活性有效部位的筛选研究[J].食品研究与开发,2021,42(06):119-123.
- 37. 陈丰,陈志清,钟桂玲,王贺,朱继金.葛根素预处理对心肌梗死模型大鼠HMGB1的表达及心肌细胞凋亡的影响[J].广西医科大学学报,2020,37(08):1404-1409.
- 36. 杨梦玲, 尤朋涛, 何丽珊,等. 基于UPLC-MS/MS分析胃溃疡模型大鼠口服加味小柴胡颗粒后血浆中8种有效成分的药代动力学[J]. 中国中药杂志, 2018, 43(18).
- 35. 任丽, 贾田芊, 李兴欢,等. 黄花油点草药材的质量标准研究[J]. 中国药房, 2019, 030(008):1083-1090.
- 34. 侯景龙, 毛跟年, 胡媛,等. 葛根,枳椇子解酒组合物体外抗氧化活性的研究[J]. 动物医学进展, 2020, 041(002):63-69.
- 33. 牛晓静, 曹英杰, 段晓颖. 多指标正交试验优选通络调脂胶囊提取工艺[J]. 中药新药与临床药理, 2015, 026(006):851-854.
- 32. 潘洁, 杨淑婷, 孙佳, et al. 荭草中6种活性成分在正常和心肌缺血模型大鼠体内的肠吸收特征差异研究[J]. 中国药房, 2020(13).
- 31. 吴文杰 邓阳 谭桂林 罗娟 陈秧 黄莺 张峰.一测多评法测定葛根药材中5种异黄酮类成分[J].中草药 2017 48(04):777-781.
- 30. 黄仁术, 胡晓梦, 何惠利. 大别山野葛根异黄酮超声辅助提取工艺的响应面优化与还原力测定[J]. 中国药学杂志, 2015, 50(001):51-57.
- 29. 李玲, 全沁果, 沈艳欣, et al. 野葛藤地上部分葛根素的提取及稳定性研究[J]. 食品工业科技, 2016, 37(9):235-239.
- 28. 李玲, 郭慧, 何福林,等. 野葛花葛根素的提取及稳定性研究[J]. 中国食品添加剂, 2017(3).
- 27. 李玲, 谭力, 全沁果,等. 野葛块根异黄酮的提取及抗氧化研究[J]. 浙江农业学报, 2016, v.28;No.160(03):496-501.
- 26. 严航, 杨晶, 唐婷,等. 葛根黄酮脂质体的制备及体外透皮实验研究[J]. 中成药, 2014, 36(003):623-625.
- 25. 桂卉,唐婷,严航,雷志钧.葛根黄酮类物质美白作用的研究[J].日用化学工业,2013,43(04):290-293+312.
- 24. 胡亚丽,杨杰,庞茜茜.葛根素通过PTEN/PI3K/Akt通路调控人肝癌HepG2细胞增殖和凋亡的研究[J].现代消化及介入诊疗,2020,25(07):883-888.
- 23. 王帅, 李清清, 王帆,等. 葛根素药物纳米晶自稳定pickering乳的大鼠肠吸收特性研究[J]. 中国中药杂志, 2018, v.43(10):212-217.
- 22. 王晶, 李洪敏, 艾芳,等. 葛根素的提取及对小鼠解酒护肝功能的鉴定[J]. 局解手术学杂志, 2015(04):358-361.
- 21. 陈媛, 吴海金, 黄晓松,等. 葛根素对脑缺血再灌注大鼠海马组织P-STAT3、P53表达的影响[J]. 湖南中医药大学学报, 2018, 038(001):36-39.
- 20. 张晓丹, 杜伟, 张晨,等. 葛根素对缺氧性肺动脉高压及伴随的肺纤维化的作用[J]. 中国中药杂志, 2018, 43(12).
- 19. 陈媛, 黄晓松, 吴海金,等. 葛根素对大鼠脑缺血再灌注损伤后JAK2/STAT3信号通路的影响[J]. 湖南中医杂志, 2017, 04(v.33;No.218):149-152+170.
- 18. 刘银莉, 王营. 葛根素对人胰腺癌PANC-1细胞增殖凋亡的影响[J]. 实用药物与临床, 2017(11):20-24.
- 17. 宋逍, 段玺, 徐萌,等. 葛根中有效成分葛根素膜分离工艺研究[J]. 时珍国医国药, 2019(10).
- 16. ]滕飞[1], 李博[1], 谢静[1],等. 葛根中抑制磷酸二酯酶4活性成分的筛选研究[J]. 分子科学学报(中,英文), 2018(1).
- 15. 陈松旺, 吴婷, 李煌,等. 畅脉乐胶囊的质量标准研究[J]. 福建医药杂志, 2020, 042(001):127-132.
- 14. 温海成, 杨颖欣, 叶信,等. 正交试验优选壮药三裂叶葛藤中葛根素的提取工艺研究[J]. 中国民族医药杂志, 2016(9).
- 13. 晏雨露, 徐驿, 赵继会,等. 微针辅助条件下葛根素微乳的经皮吸收研究[J]. 中草药, 2017, 048(001):95-101.
- 12. 李博,赵安琦,张慧荣,李丽.应用超滤液相色谱和电喷雾质谱技术筛选MMP-2活性成分[J].分子科学学报,2015,31(02):94-100.
- 11. 马晓云,刘洋,杨瑞瑞,罗志强,鲁利娜,赵海誉,赵慧辉.封闭肠环法用于葛根多成分肠壁吸收代谢研究[J].中国中药杂志,2017,42(08):1532-1538.
- 10. 杨玉琴, 昶国平, 张志超,等. 复方丹参保肝颗粒入血成分研究[J]. 现代中药研究与实践, 2016, 030(003):37-40.
- 9. 陆苑,黎娜,刘春花,潘洁,李勇军,王永林,孙佳.基于在体肠袢模型研究荭草活性成分在正常及心肌缺血模型大鼠的肠吸收特性[J].中国药理学通报,2020,36(08):1146-1151.
- 8. 陈程,罗国平,冯锁民,张存劳,闫梦茹,郭艳茹.基于PB设计和BBD响应面法优化葛根-黄连药对提取工艺[J].中国药师,2018,21(02):228-231.
- 7. 罗静, 陈诗晴, 李玉锋,等. 基于Box-Behnken设计优化复方葛根黄酮泡腾片的制备工艺研究[J]. 食品工业, 2018, v.39;No.262(07):175-180.
- 6. 王京龙, 郑丹丹, 王磊,等. 均匀设计法优化葛根半仿生提取工艺[J]. 中成药, 2017(5).
- 5. 卜雕雕 张丹 王昌利. 响应面法优化药对葛根-川芎提取工艺[J]. 辽宁中医药大学学报 2019 021(004):54-57.
- 4. 黄仁术 孙峥峥 何惠利. 响应面法优化大别山野葛根多糖提取工艺研究[J]. 药物生物技术 2015 022(001):59-63.
- 3. 昶国平 魏雅蕾 林宏英 等. 丹葛保肝复方提取工艺的研究[J]. 中医药学报 2015(03):76-78.
- 2. 张丽娟 李燕 周剑丽 等. 一种降糖代餐粉的配方研究及质量评价[J]. 食品研究与开发 2019 40(09):105-110.
- 1. 崔灵 张丽姝 陈萌萌 等. HPLC法同时测定知葛胶囊中葛根素、马钱苷、芒果苷以及芦丁的含量[J]. 沈阳药科大学学报 2018(7).







 浙公网安备 33010802013016号
浙公网安备 33010802013016号